Scienza e curiosità del Lago di Garda #5 di Claire Beaux
Ossigeno, azoto, ferro, potassio, manganese e tanti altri sono i 92 elementi naturali (più una serie di elementi artificiali) che compongono la tavola periodica, oggetto di “culto” di tutti i chimici. Elementi, alcuni, essenziali per la vita, altri impiegati in tecnologia, altri pericolosi. Parlare di chimica non sempre significa “tossicità e danno”, anzi, come ben sappiamo l’ossigeno è fondamentale per gli esseri viventi. La sua presenza nelle acque del Lago, alle diverse profondità, permette lo sviluppo di varie specie, vegetali e animali.
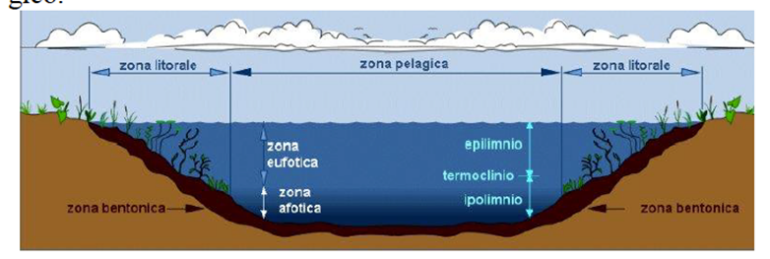
Nel Lago si distinguono due zone con caratteristiche diverse:
- zona eufotica (dal greco photòs = luce): raggiunta dai raggi solari, qui si ha la produzione di ossigeno per fotosintesi;
- zona afotica: negli strati più profondi, dove la luce solare non arriva, qui si ha il consumo di ossigeno
Ossigeno
L’ossigeno è presente nelle acque in bassa concentrazione e il maggior apporto di tale elemento proviene dall’atmosfera e dai processi di fotosintesi dei vegetali in esse presenti. La quantità di gas proveniente dall’aria dipende dalla sua capacità di dissolversi (legge di Henry e Dalton, ben note a noi sub), dall’altitudine (esiste una relazione fra pressione barometrica e pressione parziale dell’ossigeno) e dall’umidità dell’aria (l’acqua di superficie ha la capacità di diluire i gas, ma dipende dalla sua tensione superficiale). Naturalmente i vegetali, i processi chimici di trasformazione dei minerali (ossidazione) e i batteri influiscono sulla concentrazione dell’ossigeno, che si distribuisce lungo la colonna d’acqua in base ai moti turbolenti e alle variazioni di temperatura. Le attività biologiche danno un contributo notevole soprattutto nel periodo di stratificazione estiva: nelle parte più bassa dell’epilimnio e negli strati più superficiali del metalimnio, la produzione di ossigeno può essere addirittura maggiore del consumo del gas. Tale fenomeno dipende comunque dal tipo di lago.
Il monitoraggio dell’ossigeno permette di capire lo stato di (eventuale) inquinamento del bacino lacustre: troppo ossigeno alla superficie ha come effetto un’eccessiva attività fotosintetica che può compromettere l’equilibrio dell’ecosistema (eutrofizzazione). Di conseguenza, sul fondo, il gas diminuisce, quasi fino a una situazione di anossia (assenza di ossigeno).
Azoto
Noi sub lo associamo alla narcosi da azoto e alle pericolose bolle, è quindi un “nemico”? In realtà, questo gas è il componente essenziale di proteine, acidi nucleici e altri costituenti le cellule, quindi potremmo quasi azzardare no azoto, no vita. L’azoto si trova sia disciolto in acqua, sia nei composti in essa presenti: raggiunge l’elemento lacustre grazie alle piogge e i bacini imbriferi (ossia i bacini di raccolta delle acque piovane e fluviali che circondano un lago) e, non da ultimo, dalla fissazione da parte di alcuni batteri.
Queste azioni chimiche sono fondamentali perché l’azoto è un gas inerte, ha quindi bisogno di essere “lavorato” perché si renda utile.
Anidride carbonica (CO2) e pH
L’anidride carbonica si discioglie in acqua, reagisce con essa ed è presente in maniera sostanziosa. Pioggia, decomposizione delle sostanze organiche, respirazione degli organismi acquatici, acque sotterranee. La CO2 assorbita dalle alghe viene convertita in carboidrati utili per “creare” sostanze di nutrimento che vengono assimilate dagli animali che si nutrono delle alghe stesse. Tali animali, con la respirazione, riemettono la CO2 e il ciclo ricomincia. Le attività di tipo biologico, producendo e consumando anidride carbonica, modificano il pH (concentrazione idrogenionica) delle acque: dal suo valore dipende la possibilità o meno di insediamenti floro-faunistici.

Fosforo
È un elemento molto abbondante nella materia organica ed è chiamato anche nutriente algale perché è fondamentale per la crescita delle alghe e il processo della fotosintesi. Si presenta sciolto in acqua, in sospensione e in particelle organiche. La sua concentrazione varia da bacino a bacino e la sua quantità è un indicatore dell’inquinamento dovuto a uso di fertilizzanti agricoli, scarichi urbani e industriali. Molti altri elementi sono presenti nelle acque lacustri: il calcio è essenziale per la maggior parte delle piante acquatiche perché anch’esso è coinvolto nella fotosintesi clorofilliana, silicio e silicati sono impiegati dalle Diatomee, alghe formate da cellule protette da un guscio siliceo, sodio e potassio che compongono rocce e fondale.
In ultimo dobbiamo ricordare la sostanza organica, ossia sostanza, in genere presente in sospensione e in soluzione, prodotta da tutte le attività biologiche che avvengono nel lago (sono dette autoctone) e quelle provenienti dal bacino imbrifero (dette alloctone). Delle sostanze autoctone fanno parte i secreti degli organismi, quali feci e sostanze rilasciate dalla decomposizione; quelle alloctone possono derivare dal dilavamento dei suoli, dai rifiuti, quindi possono contenere anche elementi organici di sintesi e non naturali. La chimica e i suoi elementi regolano le popolazioni lacustri sia perché forniscono loro nutrimento sia perché ne possono determinare un particolare incremento.
La vita è un ciclo, si sa: il plancton ha vita breve, appena dopo la sua morte comincia la mineralizzazione della sostanza organica, di questa si nutrono i batteri che emettono anidride carbonica, sali, ammoniaca così da fornire ai produttori primari (i vegetali) molecole semplici per dare il via alla fotosintesi che rilascia ossigeno senza il quale la vita non sarebbe possibile. E il ciclo si chiude per ricominciare.
Fonti
V. Tonolli Introduzione allo studio della limnologia (1964)
R. Bertoni Laghi e scienza (2018)




